| Virus BK | |
|---|---|
 |
|
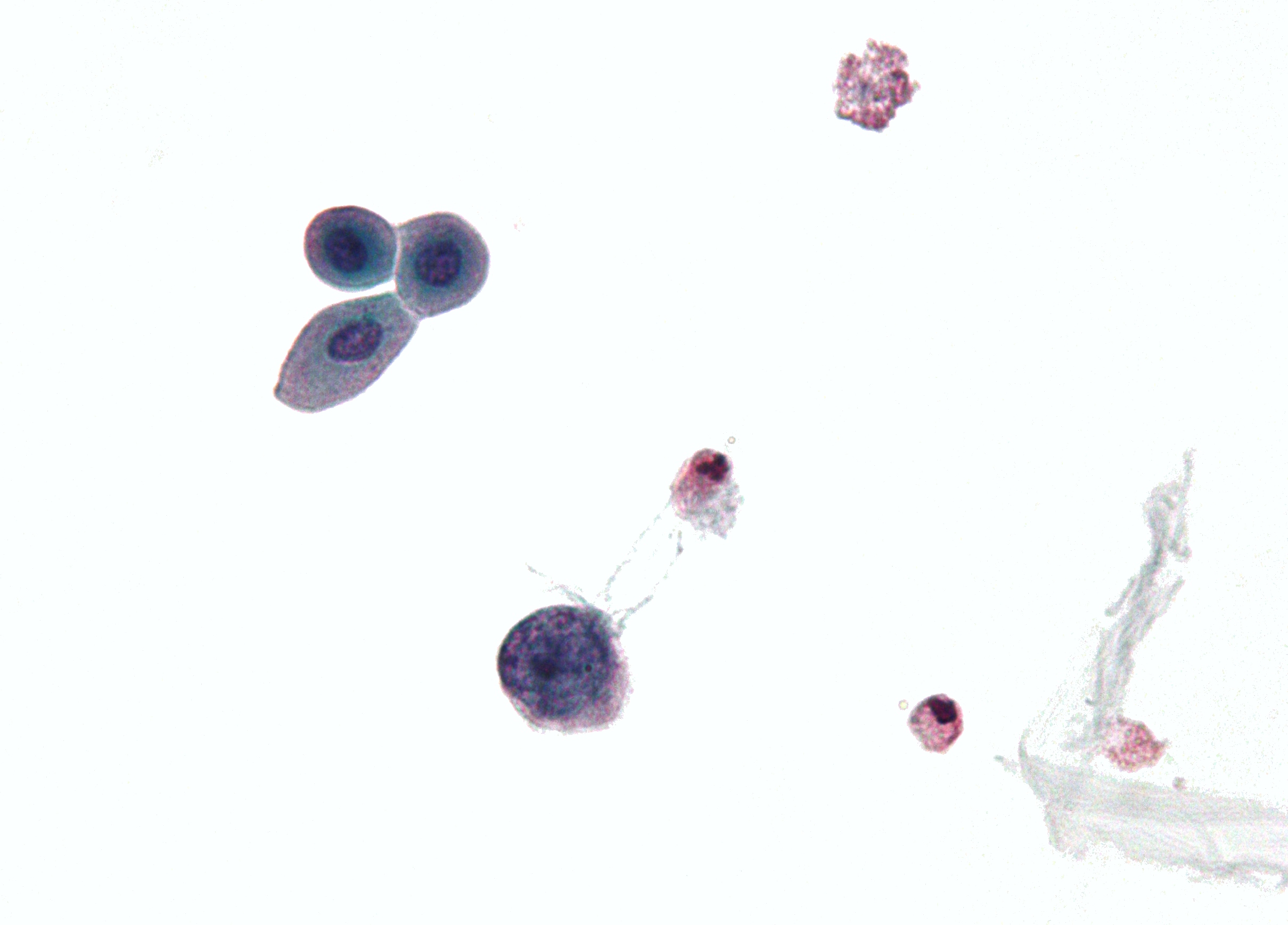
| Micrografía que muestra una célula infectada por un poliomavirus — célula grande (azul) en el centro inferior izquierda. Especimen de citología urinaria. | |
| Especialidad | Enfermedades infecciosas |
El virus BK es un miembro de la familia de los poliomavirus. La infección por el virus BK es común, pero las consecuencias significativas de la infección son poco comunes, excepto en personas inmunocomprometidas e inmunosupuestas. El virus BK es una abreviatura del nombre del primer paciente del cual se aisló el virus en 1971 (el paciente tenía entonces 29 años).
Síntomas de la infección por virus BK
El virus BK raramente causa enfermedad, pero se asocia típicamente con pacientes que han tenido un trasplante de riñón; muchas personas infectadas con este virus son asintomáticas. Si aparecen síntomas, tienden a ser leves: infección respiratoria o fiebre. Estos son síntomas de infecciones primarias por BK. Aunque sin ningún síntoma clínico, se han detectado huellas del virus BK en especímenes de mujeres afectadas por aborto espontáneo. También se han encontrado anticuerpos en suero contra el virus BK en mujeres que han sufrido aborto espontáneo y en mujeres que se sometieron a interrupción voluntaria del embarazo.
Luego, el virus se disemina a los riñones y al tracto urinario, donde persiste durante la vida del individuo. Se piensa que hasta el 80% de la población tiene una forma latente de este virus, que permanece latente hasta que el cuerpo experimenta alguna forma de inmunosupresión. Típicamente, esto ocurre en el contexto del trasplante renal o del trasplante multiorgánico. La presentación en estas personas inmunocomprometidas es mucho más grave. Las manifestaciones clínicas incluyen disfunción renal (observada por un aumento progresivo de la creatinina sérica) y un análisis de orina anormal que revela células tubulares renales y células inflamatorias.
Causa de la infección por virus BK
Transmisión del virus
Los médicos no saben cómo se transmite este virus. Pero saben que el virus se propaga de persona a persona, y no de una fuente animal. Se ha sugerido que este virus puede ser transmitido a través de fluidos respiratorios o de la orina, ya que los individuos infectados excretan periódicamente virus en la orina. Una encuesta de 400 donantes de sangre sanos mostró que el 82% era positivo para IgG contra el virus BK.
Factores de riesgo
En algunos pacientes con trasplante renal, el uso necesario de medicamentos inmunosupresores tiene el efecto secundario de permitir que el virus se replique dentro del injerto, una enfermedad llamada nefropatía por virus BK.
Del 1 al 10% de los pacientes de trasplante renal progresan a nefropatía asociada al virus BK (BKVAN) y hasta el 80% de estos pacientes pierden sus injertos. El inicio de la nefritis puede ocurrir desde unos días después del trasplante hasta 5 años después.
También se relaciona con estenosis ureteral y nefritis intersticial. En receptores de trasplante de médula ósea, es notable como causa de cistitis hemorrágica.
Carga de viremia de BK > 185,000 copias/ml en el momento del primer diagnóstico positivo de BKV se considera el predictor más fuerte para BKVAN (97% de especificidad y 75% de sensibilidad). Además, se encontró que las cargas virales picos de BKV en sangre que alcanzaron 223,000 copias/ml en cualquier momento eran predictivas para BKVAN (91% de especificidad y 88% de sensibilidad).
Diagnóstico de la infección por virus BK
Este virus puede ser diagnosticado mediante un análisis de sangre de BKV o un examen de orina en busca de células decoy, además de llevar a cabo una biopsia en los riñones. Se suelen realizar técnicas de PCR para identificar el virus.
Tratamiento de la infección por virus BK
La piedra angular de la terapia es la reducción de la inmunosupresión. Un reciente aumento en BKVAN se correlaciona con el uso de potentes inmunosupresores, como tacrolimus y mofetil micofenolato (MMF). Los estudios no han mostrado ninguna correlación entre BKVAN y un único agente inmunosupresor, sino más bien con la carga inmunosupresora total.
- No existen guías ni niveles o dosis de medicamentos para una adecuada reducción de inmunosupresores en BKVAN
- Métodos más comunes:
- Retirada de MMF o tacrolimus
- Sustitución de tacrolimus por ciclosporina
- Reducción general de la carga inmunosupresora
- Se ha informado que algunos niveles de ciclosporina en el mínimo han sido reducidos a 100–150 ng/ml y niveles de tacrolimus a 3–5 ng/ml
- Un análisis retrospectivo de 67 pacientes concluyó que la supervivencia del injerto fue similar entre la reducción y la discontinuación de los agentes.
- Un estudio de un solo centro mostró que los injertos renales fueron preservados en 8 de 8 individuos manejados con reducción de la inmunosupresión, mientras que la pérdida del injerto ocurrió en 8 de 12 pacientes tratados con un aumento de la terapia por lo que se pensó que era un rechazo del órgano.
Otras opciones terapéuticas incluyen Leflunomida, Cidofovir, IVIG y fluoroquinolonas. La leflunomida, un inhibidor de la síntesis de pirimidina, es ahora generalmente aceptada como la segunda opción de tratamiento detrás de la reducción de la inmunosupresión.
Leflunomida en BKVAN
La justificación para usar leflunomida en BKVAN proviene de sus propiedades inmunosupresoras y antivirales combinadas. Dos estudios que incluyeron a 26 y 17 pacientes que desarrollaron BKVAN bajo un régimen de tres fármacos de tacrolimus, MMF y esteroides reemplazaron su MMF por leflunomida entre 20 y 60 mg diarios. El 84% y 88% de los pacientes, respectivamente, tuvieron una eliminación o reducción progresiva de la carga viral y una estabilización o mejora de la función del injerto. En un estudio realizado por Teschner et al. en 2009, 12 de 13 pacientes que tuvieron su MMF intercambiado por leflunomida eliminaron el virus en 109 días. En una serie de casos, hubo mejora o estabilización en 23 de 26 pacientes con BKVAN después de cambiar de MMF a leflunomida.
No existen guías de dosificación para leflunomida en BKVAN. La variabilidad entre pacientes ha hecho que la dosificación y el monitoreo de leflunomida sean extremadamente difíciles.
- Estudios de 26 y 17 pacientes fueron dosificados entre 20 mg/día y 60 mg/día con niveles mínimos de 50-100 µg/ml. El fracaso se observó en pacientes con niveles plasmáticos de leflunomida < 40 µg/ml.
- Un estudio de 21 pacientes encontró que los niveles bajos (< 40 µg/ml) y los niveles altos (> 40 µg/ml) tuvieron efectos similares en la tasa de eliminación viral. Aquellos con niveles más altos tuvieron más eventos adversos (hematológicos, hepáticos).
- En el estudio de Teschner et al., las dosificaciones y concentraciones de medicamentos no mostraron correlación con una variación sustancial de persona a persona.
- En el estudio de Teschner, se asoció una baja concentración del fármaco con la disminución de la carga viral. Esto dificulta determinar si la reducción de la carga viral o la adición de leflunomida fue la causa de la eliminación viral.
Otras opciones de tratamiento
- Antibióticos quinolónicos: se demostró que la ciprofloxacina (Cipro) disminuyó significativamente las cargas virales, pero no existen datos sobre la supervivencia y la pérdida del injerto.
- La inmunoglobulina intravenosa (IVIG) tiene uso en el tratamiento de infecciones y rechazo de injertos — difícil de distinguir.
- El cidofovir tiene datos limitados y es altamente nefrotóxico.
Historia
El virus BK fue aislado por primera vez en 1971 de la orina de un paciente con trasplante renal, iniciales B.K. El virus BK es similar a otro virus llamado el virus JC (JCV), ya que sus genomas comparten un 75% de similitud en la secuencia. Ambos de estos virus pueden ser identificados y diferenciados entre sí realizando pruebas serológicas utilizando anticuerpos específicos o mediante un enfoque de tipificación por PCR.